ມັນເປັນສິ່ງ ສຳ ຄັນຫຼາຍທີ່ຈະຕ້ອງເຂົ້າໃຈວ່າການສັງເຄາະຂອງຄໍເລສເຕີຣອນໃນຕັບເກີດຂື້ນແນວໃດ ຖ້າທ່ານກວດສອບບັນຫານີ້ຢ່າງລະອຽດ, ມັນຈະກາຍເປັນທີ່ຈະແຈ້ງວ່າຕັບມີສ່ວນພົວພັນກັບສານອິນຊີຊະນິດນີ້ແນວໃດ. ແຕ່ ທຳ ອິດທ່ານ ຈຳ ເປັນຕ້ອງຈື່ວ່າສານດັ່ງກ່າວຍັງມີຊື່, ເຊິ່ງມັນຍັງຖືກ ນຳ ໃຊ້ເລື້ອຍໆ, ແມ່ນຄໍເລດເຕີລອນ.
ດັ່ງທີ່ໄດ້ກ່າວມາແລ້ວຂ້າງເທິງ, ສານນີ້ແມ່ນສານປະສົມສານອິນຊີແລະມີຢູ່ໃນທຸກສິ່ງມີຊີວິດ. ມັນແມ່ນສ່ວນປະກອບ ໜຶ່ງ ຂອງ lipids.
ຄວາມເຂັ້ມຂົ້ນສູງສຸດແມ່ນສັງເກດເຫັນໃນຜະລິດຕະພັນຕົ້ນ ກຳ ເນີດຂອງສັດ. ແຕ່ໃນຜະລິດຕະພັນພືດມີພຽງແຕ່ສ່ວນນ້ອຍຂອງສານປະສົມນີ້ເທົ່ານັ້ນ.
ມັນຍັງມີຄວາມສໍາຄັນທີ່ຈະສັງເກດຄວາມຈິງທີ່ວ່າຄຽງຄູ່ກັບອາຫານພຽງແຕ່ 20 ສ່ວນຮ້ອຍຂອງຈໍານວນໄຂມັນທີ່ເຂົ້າໄປ, ສ່ວນທີ່ເຫຼືອ 80 ສ່ວນຮ້ອຍຂອງຮ່າງກາຍຈະຜະລິດເອກະລາດ. ໂດຍວິທີທາງການ, ຂອງສານສັງເຄາະທັງ ໝົດ ຢ່າງດຽວ, 50% ແມ່ນຖືກສ້າງຕັ້ງຂຶ້ນໂດຍກົງໃນຕັບ. ສິ່ງນີ້ເກີດຂື້ນໃນລະດັບເຊນ, ສ່ວນທີ່ເຫລືອ 30% ແມ່ນຜະລິດຢູ່ໃນ ລຳ ໄສ້ແລະຜິວ ໜັງ.
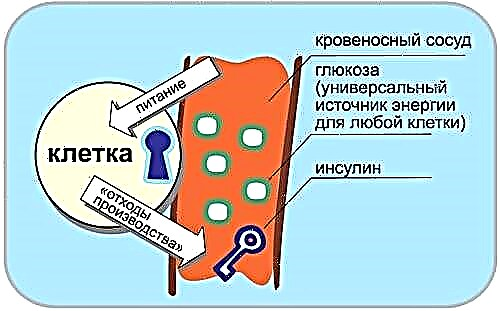
ຮ່າງກາຍຂອງມະນຸດມີຫຼາຍຊະນິດຂອງສ່ວນປະກອບນີ້. ໃນເວລາດຽວກັນ, ຄວນສັງເກດວ່າມັນແມ່ນລະບົບ hematopoietic ທີ່ອີ່ມຕົວກັບສານນີ້. Cholesterol ໃນເລືອດແມ່ນສ່ວນ ໜຶ່ງ ຂອງທາດປະສົມທີ່ສັບສົນກັບທາດໂປຼຕີນ, ສະລັບສັບຊ້ອນດັ່ງກ່າວເອີ້ນວ່າ lipoproteins.
ສະລັບສັບຊ້ອນສາມາດຂອງສອງປະເພດ:
- HDL - ມີຄວາມຫນາແຫນ້ນສູງຫຼາຍ, ພວກມັນຖືກເອີ້ນວ່າດີ;
- LDL - ມີຄວາມ ໜາ ແໜ້ນ ຕ່ ຳ, ສານເຫຼົ່ານີ້ເອີ້ນວ່າບໍ່ດີ.
ມັນແມ່ນປະເພດທີສອງທີ່ ນຳ ເອົາຄວາມອັນຕະລາຍມາສູ່ມະນຸດ. ຫຼັງຈາກທີ່ພວກມັນຕົກຄ້າງ, ເຊິ່ງປະກອບດ້ວຍໄປເຊຍກັນຂອງສານ, ພວກມັນເລີ່ມສະສົມໃນຮູບແບບຂອງແຜ່ນຢູ່ຕາມຝາຂອງເສັ້ນເລືອດຂອງລະບົບການໄຫຼວຽນ, ມີຄວາມຮັບຜິດຊອບໃນການຂົນສົ່ງເລືອດ. ດັ່ງນັ້ນ, ຂະບວນການນີ້ຈະກາຍເປັນສາເຫດຂອງການພັດທະນາໃນຮ່າງກາຍຂອງພະຍາດທາງດ້ານພະຍາດດັ່ງກ່າວເປັນໂຣກ atherosclerosis.
ຄວາມຄືບຫນ້າຂອງໂຣກ atherosclerosis ເຮັດໃຫ້ການພັດທະນາຂອງພະຍາດທີ່ຮ້າຍແຮງຫຼາຍ.
ລັກສະນະການເຊື່ອມຕໍ່ພື້ນຖານ
ດັ່ງທີ່ໄດ້ກ່າວມາຂ້າງເທິງ, ສານນີ້ສາມາດເປັນປະໂຫຍດ ສຳ ລັບມະນຸດ, ແນ່ນອນ, ຖ້າພວກເຮົາ ກຳ ລັງເວົ້າເຖິງ HDL ເທົ່ານັ້ນ.
ອີງໃສ່ສິ່ງນີ້, ມັນຈະກາຍເປັນທີ່ຈະແຈ້ງວ່າການຢືນຢັນວ່າຄໍເລສເຕີໂຣນແມ່ນເປັນອັນຕະລາຍແທ້ໆຕໍ່ມະນຸດແມ່ນຄວາມຜິດພາດ.
Cholesterol ແມ່ນສ່ວນປະກອບທີ່ເຮັດວຽກທາງຊີວະພາບ:
- ມີສ່ວນຮ່ວມໃນການສັງເຄາະຮໍໂມນເພດ;
- ຮັບປະກັນການເຮັດວຽກປົກກະຕິຂອງ receptors serotonin ໃນສະ ໝອງ;
- ແມ່ນສ່ວນປະກອບຫຼັກຂອງ ໜິ້ວ ນໍ້າບີ, ເຊັ່ນດຽວກັນກັບວິຕາມິນດີ, ເຊິ່ງມີ ໜ້າ ທີ່ຮັບຜິດຊອບຕໍ່ການດູດຊຶມຂອງໄຂມັນ;
- ປ້ອງກັນບໍ່ໃຫ້ຂະບວນການ ທຳ ລາຍໂຄງສ້າງພາຍໃຕ້ອິດທິພົນຂອງອິດສະຫຼະອິດສະຫຼະ.
ແຕ່ຄຽງຄູ່ກັບຄຸນລັກສະນະໃນທາງບວກ, ສານດັ່ງກ່າວສາມາດມີຜົນກະທົບບາງຢ່າງຕໍ່ສຸຂະພາບຂອງມະນຸດ. ຍົກຕົວຢ່າງ, LDL ສາມາດເຮັດໃຫ້ເກີດການພັດທະນາຂອງພະຍາດຮ້າຍແຮງ, ປະກອບສ່ວນຕົ້ນຕໍເຂົ້າໃນການພັດທະນາຂອງໂລກ atherosclerosis.
ຢູ່ໃນຕັບ, ສານເຄມີຊີວະພາບຖືກສັງເຄາະພາຍໃຕ້ອິດທິພົນຂອງ HMG ທີ່ຖືກປັບ ໃໝ່. ນີ້ແມ່ນ enzyme ຕົ້ນຕໍທີ່ກ່ຽວຂ້ອງກັບ biosynthesis. ການຍັບຍັ້ງການສັງເຄາະເກີດຂື້ນພາຍໃຕ້ອິດທິພົນຂອງຄວາມຄິດເຫັນໃນແງ່ລົບ.
ຂະບວນການຂອງການສັງເຄາະສານໃນຕັບມີການພົວພັນກັນກັບປະລິມານສານປະສົມທີ່ເຂົ້າສູ່ຮ່າງກາຍຂອງມະນຸດກັບອາຫານ.
ເຖິງແມ່ນວ່າງ່າຍດາຍ, ຂະບວນການນີ້ຖືກອະທິບາຍດ້ວຍວິທີນີ້. ຕັບຄວບຄຸມລະດັບ cholesterol ເປັນອິດສະຫຼະ. ຄົນເຮົາບໍລິໂພກອາຫານທີ່ມີສ່ວນປະກອບນີ້ຫຼາຍເທົ່າໃດ, ສານກໍ່ຈະຖືກຜະລິດ ໜ້ອຍ ລົງໃນຈຸລັງຂອງອະໄວຍະວະແລະຖ້າເຮົາ ຄຳ ນຶງເຖິງວ່າໄຂມັນບໍລິໂພກຮ່ວມກັນກັບຜະລິດຕະພັນທີ່ບັນຈຸມັນ, ຂະບວນການກົດລະບຽບນີ້ແມ່ນມີຄວາມ ສຳ ຄັນຫຼາຍ.
ລັກສະນະຂອງການສັງເຄາະສານ
ຜູ້ໃຫຍ່ທີ່ມີສຸຂະພາບດີປົກກະຕິສັງເຄາະ HDL ໃນອັດຕາປະມານ 1 g / ມື້ແລະບໍລິໂພກປະມານ 0.3 g / ມື້.
 ລະດັບທີ່ຂ້ອນຂ້າງຂອງ cholesterol ໃນເລືອດມີຄຸນຄ່າດັ່ງກ່າວ - 150-200 mg / dl. ຮັກສາໄວ້ເປັນສ່ວນໃຫຍ່ໂດຍຄວບຄຸມລະດັບການສັງເຄາະຂອງໂດໂຊໂວ.
ລະດັບທີ່ຂ້ອນຂ້າງຂອງ cholesterol ໃນເລືອດມີຄຸນຄ່າດັ່ງກ່າວ - 150-200 mg / dl. ຮັກສາໄວ້ເປັນສ່ວນໃຫຍ່ໂດຍຄວບຄຸມລະດັບການສັງເຄາະຂອງໂດໂຊໂວ.
ມັນເປັນສິ່ງສໍາຄັນທີ່ຈະສັງເກດວ່າການສັງເຄາະຂອງ HDL ແລະ LDL ຂອງຕົ້ນກໍາເນີດທີ່ເປັນສານ endogenous ແມ່ນຖືກຄວບຄຸມໂດຍບາງສ່ວນໂດຍອາຫານ.
Cholesterol ທັງຈາກອາຫານແລະສັງເຄາະໃນຕັບແມ່ນໃຊ້ໃນການສ້າງເຍື່ອ, ໃນການສັງເຄາະຮໍໂມນສະເຕີຣອຍແລະກົດອາຊິດບີ. ອັດຕາສ່ວນທີ່ໃຫຍ່ທີ່ສຸດຂອງສານແມ່ນໃຊ້ໃນການສັງເຄາະອາຊິດບີ.
ການໄດ້ຮັບສານ HDL ແລະ LDL ໂດຍຈຸລັງຖືກຮັກສາໄວ້ໃນລະດັບທີ່ ໝັ້ນ ຄົງໂດຍ 3 ກົນໄກທີ່ແຕກຕ່າງກັນ:
- ລະບຽບການຂອງກິດຈະ ກຳ HMGR
- ກົດລະບຽບຂອງລະດັບຄໍເລດສະເຕີຣອຍຟຣີເກີນໂດຍຜ່ານກິດຈະ ກຳ ຂອງ O-acyltransferase sterol, SOAT1 ແລະ SOAT2 ກັບ SOAT2, ເຊິ່ງເປັນສ່ວນປະກອບທີ່ມີສ່ວນ ສຳ ຄັນໃນຕັບ. ການອອກແບບເບື້ອງຕົ້ນ ສຳ ລັບເອນໄຊເຫຼົ່ານີ້ແມ່ນ ACAT ສຳ ລັບ acyl-CoA: cholesterol acyltransferase. Enzymes ACAT, ACAT1, ແລະ ACAT2 ແມ່ນ acetyl CoA acetyltransferases 1 ແລະ 2.
- ໂດຍການຄວບຄຸມລະດັບ cholesterol ຂອງ plasma ຜ່ານການຮັບເອົາ LDL-mediated receptor ແລະການຂົນສົ່ງດ້ານ HDL-mediated.
ລະບຽບການຂອງກິດຈະ ກຳ HMGR ແມ່ນວິທີການຕົ້ນຕໍໃນການຄວບຄຸມລະດັບການຜະລິດຊີວະພາບຂອງ LDL ແລະ HDL.
ເອນໄຊໄດ້ຖືກຄວບຄຸມໂດຍ 4 ກົນໄກທີ່ແຕກຕ່າງກັນ:
- ຂໍ້ຫ້າມ;
- ຄວບຄຸມການສະແດງອອກຂອງເຊື້ອສາຍ;
- ອັດຕາການເຊື່ອມໂຊມຂອງ enzyme;
- phosphorylation-dephosphorylation.
ກົນໄກຄວບຄຸມສາມຢ່າງ ທຳ ອິດແມ່ນປະຕິບັດໂດຍກົງຕໍ່ສານດັ່ງກ່າວ. Cholesterol ເຮັດ ໜ້າ ທີ່ເປັນຕົວຍັບຍັ້ງການຕອບສະ ໜອງ ກັບ HMGR ທີ່ມີຢູ່ກ່ອນແລະຍັງເຮັດໃຫ້ມີການເຊື່ອມໂຊມຂອງ enzyme ຢ່າງໄວວາ. ສຸດທ້າຍແມ່ນຜົນມາຈາກການ polyubiquitilation ຂອງ HMGR ແລະການເຊື່ອມໂຊມຂອງມັນໃນໂປຣຕີນ. ຄວາມສາມາດນີ້ແມ່ນຜົນຂອງໂດເມນທີ່ລະອຽດອ່ອນຂອງ HMGR SSD.
ນອກຈາກນັ້ນ, ໃນເວລາທີ່ຄໍເລສເຕີໂຣນແມ່ນຢູ່ໃນປະລິມານທີ່ເກີນ, ປະລິມານຂອງ mRNA ສຳ ລັບ HMGR ຫຼຸດລົງເນື່ອງຈາກການສະແດງອອກຂອງເຊື້ອສາຍ.
Enzymes ມີສ່ວນຮ່ວມໃນການສັງເຄາະ
 ຖ້າສ່ວນປະກອບ exogenous ຖືກຄວບຄຸມໂດຍຜ່ານການດັດແກ້ covalent, ຂະບວນການນີ້ຈະຖືກປະຕິບັດເປັນຜົນມາຈາກ phosphorylation ແລະ dephosphorylation.
ຖ້າສ່ວນປະກອບ exogenous ຖືກຄວບຄຸມໂດຍຜ່ານການດັດແກ້ covalent, ຂະບວນການນີ້ຈະຖືກປະຕິບັດເປັນຜົນມາຈາກ phosphorylation ແລະ dephosphorylation.
ເອນໄຊແມ່ນມີການເຄື່ອນໄຫວຫຼາຍທີ່ສຸດໃນຮູບແບບທີ່ບໍ່ມີການປ່ຽນແປງ. Phosphorylation ຂອງ enzyme ຫຼຸດຜ່ອນກິດຈະກໍາຂອງມັນ.
HMGR ແມ່ນ phosphorylated ໂດຍ kinase ທາດໂປຼຕີນຈາກ AMP, AMPK. AMPK ຕົວມັນເອງຖືກກະຕຸ້ນໂດຍ phosphorylation.
phosphorylation AMPK ແມ່ນຖືກລະລາຍໂດຍຢ່າງ ໜ້ອຍ ສອງເອນໄຊ, ຄື:
- kinase ຕົ້ນຕໍທີ່ຮັບຜິດຊອບໃນການເປີດໃຊ້ AMPK ແມ່ນ LKB1 (ຕັບ kinase B1). LKB1 ໄດ້ຖືກລະບຸຕົວ ທຳ ອິດວ່າເປັນເຊື້ອສາຍໃນມະນຸດທີ່ມີການປ່ຽນແປງທີ່ໂດດເດັ່ນໃນອັດຕະໂນມັດໃນໂຣກ Putz-Jegers, PJS. LKB1 ຍັງພົບວ່າມີເຊື້ອໂຣກໃນໂຣກ adenocarcinoma.
- ທາດໂປຼຕີນຈາກ phosphorylating ທີສອງ AMPK ແມ່ນທາດໂປຼຕີນ kinase kinase beta-calmodulin ທີ່ຂື້ນກັບ calmodulin (CaMKKβ). CaMKKβກະຕຸ້ນໃຫ້ phosphorylation AMPK ໃນການຕອບສະ ໜອງ ຕໍ່ການເພີ່ມຂື້ນຂອງ Ca2 + ໃນກ້າມເຊິ່ງເປັນຜົນມາຈາກການຫົດຕົວຂອງກ້າມເນື້ອ.
ກົດລະບຽບຂອງ HMGR ໂດຍການດັດແກ້ covalent ຊ່ວຍໃຫ້ຜະລິດ HDL. HMGR ແມ່ນມີການເຄື່ອນໄຫວຫຼາຍທີ່ສຸດໃນລັດ dephosphorylated. Phosphorylation (Ser872) ແມ່ນຖືກກະຕຸ້ນໂດຍທາດໂປຼຕີນຈາກທາດໂປຼຕີນຈາກ kinase (AMPK) ທີ່ມີການເຄື່ອນໄຫວຂອງ AMP, ກິດຈະກໍາທີ່ຍັງຖືກຄວບຄຸມໂດຍ phosphorylation.
Phosphorylation ຂອງ AMPK ສາມາດເກີດຂື້ນໄດ້ຍ້ອນຢ່າງ ໜ້ອຍ ມີສອງເອນໄຊ:
- LKB1;
- CaMKKβ.
Dephosphorylation ຂອງ HMGR, ການສົ່ງມັນກັບຄືນສູ່ສະຖານະທີ່ມີການເຄື່ອນໄຫວຫຼາຍຂຶ້ນ, ແມ່ນຖືກປະຕິບັດໂດຍຜ່ານກິດຈະ ກຳ ຂອງໂປຼຕີນໂປຼຕີນຂອງຄອບຄົວ 2A. ລໍາດັບນີ້ຊ່ວຍໃຫ້ທ່ານສາມາດຄວບຄຸມການຜະລິດ HDL.
ຜົນກະທົບຕໍ່ປະເພດຂອງ cholesterol ແມ່ນຫຍັງ?
 PP2A ທີ່ມີການເຮັດວຽກມີຢູ່ໃນສອງ isoform catalytic ທີ່ແຕກຕ່າງກັນທີ່ຖືກເຂົ້າລະຫັດໂດຍສອງອະໄວຍະວະທີ່ຖືກລະບຸວ່າ PPP2CA ແລະ PPP2CB. ສອງ isoforms ຕົ້ນຕໍຂອງ PP2A ແມ່ນ enzyme ຫຼັກ heterodimeric ແລະ holoenzyme heterotrimeric.
PP2A ທີ່ມີການເຮັດວຽກມີຢູ່ໃນສອງ isoform catalytic ທີ່ແຕກຕ່າງກັນທີ່ຖືກເຂົ້າລະຫັດໂດຍສອງອະໄວຍະວະທີ່ຖືກລະບຸວ່າ PPP2CA ແລະ PPP2CB. ສອງ isoforms ຕົ້ນຕໍຂອງ PP2A ແມ່ນ enzyme ຫຼັກ heterodimeric ແລະ holoenzyme heterotrimeric.
ທາດໂປຼຕີນຈາກ PP2A ຕົ້ນຕໍແມ່ນປະກອບດ້ວຍທາດຍ່ອຍ (ທີ່ເອີ້ນວ່າ A subunit) ແລະທາດຍ່ອຍຍ່ອຍ (C subunit). ສານອະນຸມູນອິຕາລີໄດ້ຖືກເຂົ້າລະຫັດໂດຍ gene PPP2CA, ແລະທາດຍ່ອຍຍ່ອຍໄດ້ຖືກລະຫັດໂດຍ gene PPP2CB.
ພື້ນຖານໂຄງລ່າງຂອງ scaffold ແມ່ນຖືກເຂົ້າລະຫັດໂດຍ gene PPP2R1A ແລະ subnit ໂດຍ gene PPP2R1B. ທາດ enzyme ຕົ້ນຕໍ, PP2A, ພົວພັນກັບ subunit ລະບຽບການທີ່ມີຕົວປ່ຽນແປງເພື່ອປະກອບເຂົ້າໃນ holoenzyme.
ລະບົບຍ່ອຍຂອງ PP2A ລວມມີ 4 ຄອບຄົວ (ແຕ່ເດີມເອີ້ນວ່າ B-subunits), ເຊິ່ງແຕ່ລະປະກອບດ້ວຍ isoforms ຫຼາຍທີ່ຖືກເຂົ້າລະຫັດໂດຍພັນທຸ ກຳ ທີ່ແຕກຕ່າງກັນ.
ປະຈຸບັນນີ້, ມີ 15 ເຊື້ອພັນທຸ ກຳ ທີ່ແຕກຕ່າງກັນ ສຳ ລັບລະບົບຍ່ອຍຂອງ PP2A B. ໜ້າ ທີ່ຕົ້ນຕໍຂອງລະບຽບຍ່ອຍຂອງ PP2A ແມ່ນເພື່ອແນໃສ່ໂປຣຕີນຍ່ອຍ phosphorylated ສຳ ລັບກິດຈະ ກຳ phosphatase ຂອງທາດຍ່ອຍຍ່ອຍຂອງ PP2A.
PPP2R ແມ່ນ ໜຶ່ງ ໃນ 15 ອະນຸ ກຳ ມະການທີ່ແຕກຕ່າງກັນຂອງ PP2A. ຮໍໂມນເຊັ່ນ: glucagon ແລະ adrenaline ສົ່ງຜົນກະທົບຕໍ່ biosynthesis cholesterol ໂດຍການເພີ່ມກິດຈະ ກຳ ຂອງລະບົບຍ່ອຍຂອງກົດລະບຽບຂອງ PP2A ຂອງ enzymes.
PKA-mediated phosphorylation ຂອງລະບຽບການຍ່ອຍຂອງ PP2A (PPP2R) ເຮັດໃຫ້ການປ່ອຍ PP2A ອອກຈາກ HMGR, ປ້ອງກັນການລະລາຍຂອງມັນ. ໂດຍການຕ້ານກັບຜົນກະທົບຂອງ glucagon ແລະ adrenaline, insulin ກະຕຸ້ນການຂັບຖ່າຍຂອງຟອສເຟດແລະເຮັດໃຫ້ກິດຈະ ກຳ ຂອງ HMGR ເພີ່ມຂື້ນ.
ລະບຽບການເພີ່ມເຕີມຂອງ HMGR ເກີດຂື້ນໂດຍຜ່ານການສະກັດກັ້ນການຕອບສະ ໜອງ ກັບຄໍເລດເຕີລອນ, ພ້ອມທັງກົດລະບຽບຂອງການສັງເຄາະຂອງມັນໂດຍການເພີ່ມລະດັບຂອງຄໍເລດສະເຕີຣອຍແລະສະເຕີຣອຍ.
ປະກົດການສຸດທ້າຍນີ້ແມ່ນພົວພັນກັບປັດໄຈການໂອນຍ້າຍ SREBP.
ຂັ້ນຕອນໃນຮ່າງກາຍຂອງມະນຸດມີຄືແນວໃດ?
 ກິດຈະ ກຳ HMGR ຍັງຖືກຕິດຕາມກວດກາໂດຍການເຊັນສັນຍາກັບ AMP. ການເພີ່ມຂື້ນຂອງ cAMP ເຮັດໃຫ້ມີການກະຕຸ້ນຂອງ kinase ທາດໂປຼຕີນຈາກ cAMP, PKA. ໃນແງ່ຂອງລະບຽບການຂອງ HMGR, PKA phosphorylates ລະບຽບຍ່ອຍ, ເຊິ່ງເຮັດໃຫ້ການປ່ອຍ PP2A ເພີ່ມຂື້ນຈາກ HMGR. ນີ້ປ້ອງກັນ PP2A ຈາກການຖອດ phosphates ຈາກ HMGR, ປ້ອງກັນການເຮັດວຽກຂອງມັນ.
ກິດຈະ ກຳ HMGR ຍັງຖືກຕິດຕາມກວດກາໂດຍການເຊັນສັນຍາກັບ AMP. ການເພີ່ມຂື້ນຂອງ cAMP ເຮັດໃຫ້ມີການກະຕຸ້ນຂອງ kinase ທາດໂປຼຕີນຈາກ cAMP, PKA. ໃນແງ່ຂອງລະບຽບການຂອງ HMGR, PKA phosphorylates ລະບຽບຍ່ອຍ, ເຊິ່ງເຮັດໃຫ້ການປ່ອຍ PP2A ເພີ່ມຂື້ນຈາກ HMGR. ນີ້ປ້ອງກັນ PP2A ຈາກການຖອດ phosphates ຈາກ HMGR, ປ້ອງກັນການເຮັດວຽກຂອງມັນ.
ຄອບຄົວໃຫຍ່ຂອງທາດໂປຼຕີນຈາກໂປຼຕີນ phosphatase ທີ່ມີກົດລະບຽບຄວບຄຸມແລະ / ຫຼືຍັບຍັ້ງການເຄື່ອນໄຫວຂອງ phosphatases ຫຼາຍ, ລວມທັງສະມາຊິກຂອງຄອບຄົວ PP1, PP2A, ແລະ PP2C. ນອກເຫນືອໄປຈາກ phosphatases PP2A ທີ່ເອົາຟອສເຟດຈາກ AMPK ແລະ HMGR, phosphatases ຂອງໂປຼຕີນ phosphatase 2C (PP2C) ຍັງເອົາ phosphates ອອກຈາກ AMPK.
ໃນເວລາທີ່ລະບຽບການເຫຼົ່ານີ້ຍ່ອຍ phosphorylate PKA, ກິດຈະກໍາຂອງ phosphatases ຜູກພັນຫຼຸດລົງ, ເຊິ່ງເຮັດໃຫ້ AMPK ຍັງຄົງຢູ່ໃນສະພາບ phosphorylated ແລະ active, ແລະ HMGR ໃນສະພາບ phosphorylated ແລະບໍ່ມີການເຄື່ອນໄຫວ. ເມື່ອການກະຕຸ້ນຖືກຍ້າຍອອກ, ເຮັດໃຫ້ການຜະລິດ cAMP ເພີ່ມຂຶ້ນ, ລະດັບ phosphorylation ຫຼຸດລົງ, ແລະລະດັບ dephosphorylation ເພີ່ມຂື້ນ. ຜົນສຸດທ້າຍແມ່ນການກັບຄືນສູ່ລະດັບສູງຂອງກິດຈະ ກຳ HMGR. ໃນທາງກົງກັນຂ້າມ, insulin ເຮັດໃຫ້ການຫຼຸດລົງຂອງ cAMP, ເຊິ່ງ, ໃນທາງກັບກັນ, ກະຕຸ້ນການສັງເຄາະ. ຜົນສຸດທ້າຍແມ່ນການກັບຄືນສູ່ລະດັບສູງຂອງກິດຈະ ກຳ HMGR.
ໃນທາງກົງກັນຂ້າມ, insulin ເຮັດໃຫ້ການຫຼຸດລົງຂອງ cAMP, ເຊິ່ງ, ໃນທາງກັບກັນ, ກະຕຸ້ນການສັງເຄາະ cholesterol. ຜົນສຸດທ້າຍແມ່ນການກັບຄືນສູ່ລະດັບສູງຂອງກິດຈະ ກຳ HMGR. Insulin ເຮັດໃຫ້ cAMP ຫຼຸດລົງ, ເຊິ່ງໃນທາງກັບກັນ, ສາມາດຖືກນໍາໃຊ້ເພື່ອເສີມຂະຫຍາຍຂະບວນການສັງເຄາະ.
ຄວາມສາມາດໃນການກະຕຸ້ນ insulin ແລະຍັບຍັ້ງ glucagon, ກິດຈະກໍາ HMGR ແມ່ນສອດຄ່ອງກັບອິດທິພົນຂອງຮໍໂມນເຫຼົ່ານີ້ຕໍ່ກັບຂະບວນການເຜົາຜານອາຫານອື່ນໆ. ຫນ້າທີ່ຕົ້ນຕໍຂອງຮໍໂມນທັງສອງນີ້ແມ່ນເພື່ອຄວບຄຸມການເຂົ້າເຖິງແລະການຂົນສົ່ງພະລັງງານໄປຍັງຈຸລັງທັງ ໝົດ.
ການຄວບຄຸມໄລຍະຍາວຂອງກິດຈະ ກຳ HMGR ແມ່ນ ດຳ ເນີນເປັນສ່ວນໃຫຍ່ໂດຍການຄວບຄຸມການສັງເຄາະແລະການເຊື່ອມໂຊມຂອງເອນໄຊ. ເມື່ອລະດັບໄຂມັນສູງ, ລະດັບຂອງການສະແດງອອກ gene ຂອງ HMGR ຫຼຸດລົງ, ແລະໃນທາງກັບກັນ, ລະດັບຕ່ ຳ ຈະກະຕຸ້ນການສະແດງອອກຂອງ gene.
ຂໍ້ມູນກ່ຽວກັບ cholesterol ແມ່ນມີໃຫ້ໃນວີດີໂອໃນບົດຄວາມນີ້.